法规政策
-
2024.08.14
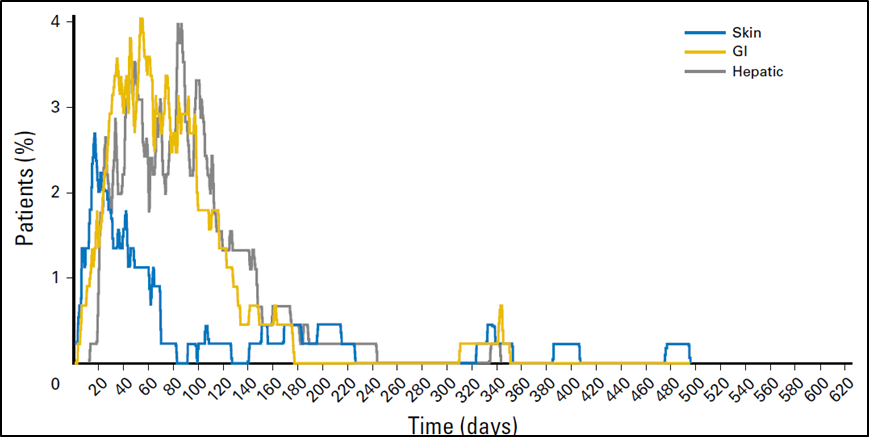
2024上海医疗设备展Medtec讲解如何应对监管机构对安全性分析的要求:临床试验中6种分析不良事件AE的方法
阅读更多 -
2024.07.23
医疗器械制造展Medtec答疑解惑-无源篇
阅读更多 -
2024.07.19
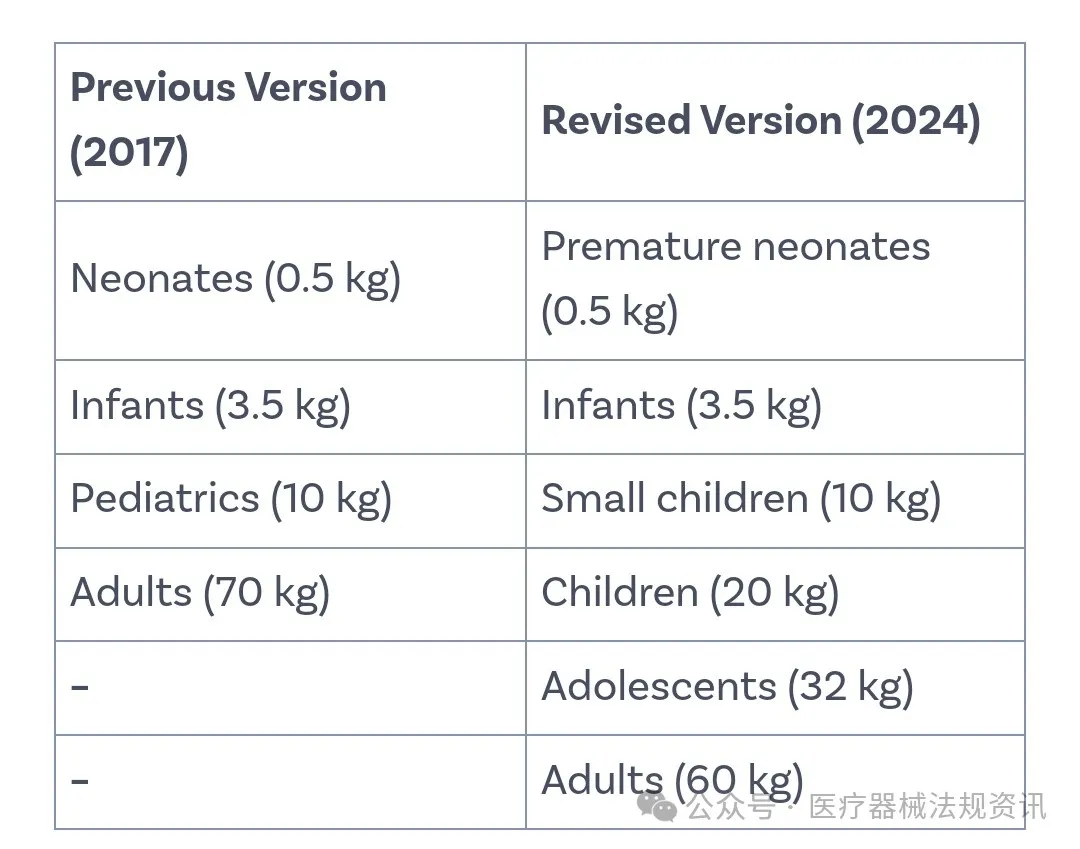
ISO 18562系列标准升版了,医疗器械制造展Medtec带你先看下 ISO 18562-1 修订内容
2024年3月,ISO 18562系列标准升版了,其中包括多项增补和变更。医疗器械制造展Medtec将利用下文重点介绍ISO 18562-1的一些重大变化。
阅读更多 -
2024.07.17
上海医疗器械展会Medtec总结如何以最高效率将MDR批准策略转移到美国市场
全球医疗器械市场面临着众多监管挑战和要求,这些挑战和要求因地区而异。其中两个重要的监管框架是欧盟的《医疗器械法规》(MDR)和美国食品药品管理局(FDA)的审批流程。这两个监管机构的主要目标都是确保医疗器械的安全性和有效性,但它们的要求和流程却大相径庭。
阅读更多 -
2024.07.13
2024上海高端医疗设备展Medtec整理最全法规标准合集,抓紧收藏!
2024上海高端医疗设备展Medtec结合医疗器械的全生命周期,将从以下六个方面来进行介绍:医疗器械的研制、注册、生产、经营、使用及监督管理。

阅读更多 -
2024.07.06
国家五部门发文!支持这些医疗器械 2024医疗器械展会Medtec盘点
2024医疗器械展会Medtec获悉,2024年6月24日,国家五部委联合发布《关于打造消费新场景培育消费新增长点的措施》,重点提出推动健康消费发展,包括研发融合数字孪生、脑机交互医疗设备和健康产品,为医疗健康指明新方向。
阅读更多 -
2024.06.23
2024医疗器械展会Medtec解读以血管内导管产品为例探讨同品种对比临床评价攻略
本文为学习性总结,如我们所知,血管内导管产品作为一大类关键医疗器械,其安全性和有效性评价一直是监管和研发的焦点。本文旨在以血管内导管为例深入解析同品种对比临床评价思路,探讨其解决的关键问题、评价思路,并通过具体情形举例,为医疗器械的临床评价提供清晰的技术路径和方法论。
阅读更多 -
2024.06.20
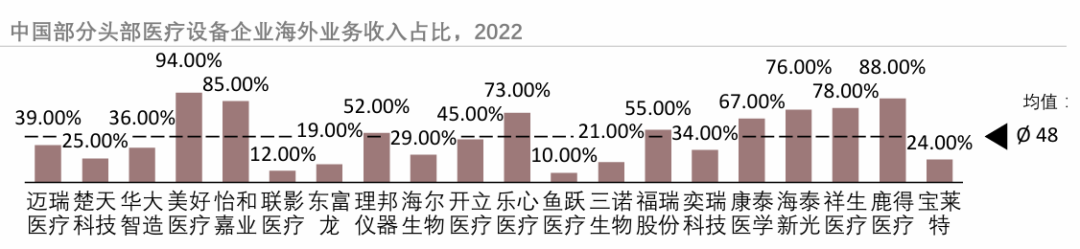
上海医疗器械博览会Medtec剖析中国医疗器械出海面临的3大挑战
中国医疗设备板块海外业务蓬勃发展,出海竞争力凸显。从医疗设备厂家出口金额角度,据Wind的数据,部分头部医疗设备上市公司的海外业务收入平均占比达到48%,整体医疗设备板块海外业务平均占比达到38.8%,其中部分企业已经形成较为成熟的海外销售体系。
阅读更多 -
2024.06.19
2024医疗器械展会Medtec解读设计开发输入对医械注册的影响
2024医疗器械展会Medtec转发本文,结合质量管理体系要求和法规要求对设计开发输入进行分析,并结合注册申报资料要求对设计开发输入给出建议。
阅读更多 -
上海医疗器械展会Medte转载-医疗器械临床试验机构监督检查新规发布,自10月1日起施行
上海医疗器械展会Medtec获悉,6月14日,国家药监局及国家药监局食品药品审核查验中心分别发布《医疗器械临床试验机构监督检查办法(试行)》《医疗器械临床试验机构监督检查要点及判定原则(试行)》。上述文件自2024年10月1日起施行。
阅读更多











